les bases scientifiques du projet
Il y a maintenant plus d’une trentaine d’années, naissait la notion d’origine développementale de la santé et des maladies (DOHaD, pour developmental origins of health and disease).
Le concept de programmation précoce.
L’épidémiologiste britannique David BARKER (1932-2013) a montré, au cours des années 80, un lien entre le risque de décès par maladie coronarienne à l’âge adulte, et le poids du sujet à sa naissance. Il s’agissait de la première liaison établie entre une exposition précoce défavorable et la survenue d’une pathologie à l’âge adulte.
Depuis de nombreux autres chercheurs ont largement confirmé ce concept de la programmation au cours du développement, du risque de maladie chronique à l’âge adulte, voire comme on le sait maintenant, d’une «transmission aux générations suivantes ». On parle de modifications épigénétiques. Les modifications moléculaires induites par l’environnement ne changent pas le code génétique mais agissent au niveau de l’expression des gènes.

L’épigénétique
L’épigénétique (du grec ancien ἐπί, épí, « au-dessus de », et de génétique) est la discipline de la biologie qui étudie la nature et les mécanismes des modifications réversibles et transmissibles lors des divisions cellulaires permettant de moduler l’expression des gènes sans en changer la séquence nucléotidique.
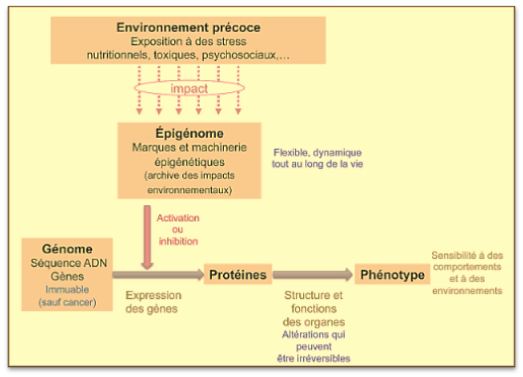
L’épigénétique constitue une passerelle entre l’environnement et le génome.
Des « bobines » de gènes.
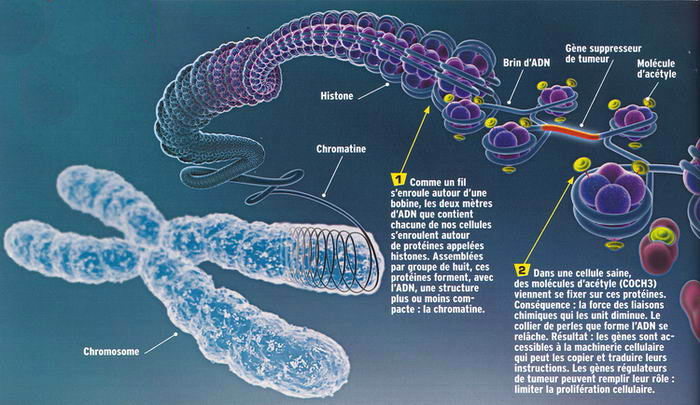
L’ADN de nos 46 chromosomes mesure 2 mètres. Afin que tout soit contenu dans le noyau d’une cellule de 10 à 100 µm de diamètre, la molécule d’ADN est enroulée autour de complexes de protéines nommées histones. Il s’agit du compactage, les structures ainsi constituées sont les nucléosomes.
Ces structures s’enroulent aussi sur elles-mêmes de manière plus ou moins serrée.
- Rendant le compactage de l’ADN élevé, dans ce cas les gènes ne sont pas accessibles et donc pas exprimés.
- Si les zones de la chromatine peu condensée, sont accessibles aux complexes enzymatiques, l’expression des gènes est possible.
Des modifications épigénétiques, affectant les histones permettent à la chromatine de passer de l’un à l’autre de ces états.
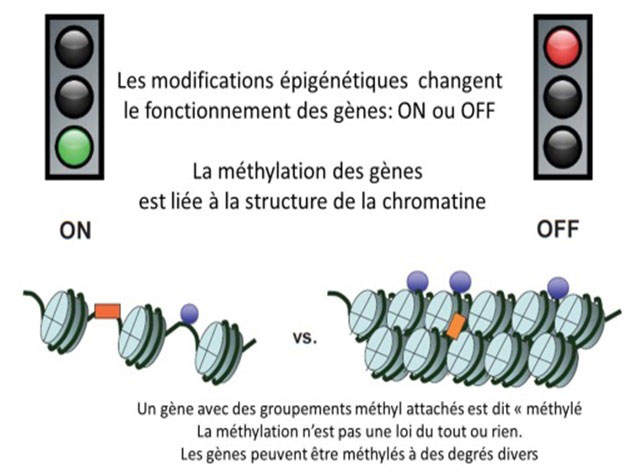
L’expression des gènes liés à l’environnement.
La cellule reçoit en permanence des informations lui permettant de répondre aux signaux de son environnement. Ces signaux, y compris ceux liés aux comportements (alimentation, tabagisme, stress, inactivité…), peuvent conduire à des modifications dans l’expression des gènes.
Il s’agit de modifications épigénétiques induites par l’environnement au sens large, qui peuvent parfois persister même lorsque le signal a cessé.
Des marques transmissibles.
Au cours du développement embryonnaire, les cellules, au départ toutes identiques, reçoivent des signaux pour activer ou inactiver certains de leurs gènes et se différencier. L’organisme se construit. Si au cours de cette période des modifications épigénétiques sont transmises au cours des divisions cellulaires, l’expression des gènes pourra être différente.
Certaines marques épigénétiques pourraient même passer à la descendance.
Un exemple est celui du gène agouti, impliqué dans la détermination de la couleur du pelage chez la souris : dans un groupe d’animaux portant tous la même version de ce gène, certains ont un pelage brun chiné et d’autre un pelage jaune. Ces derniers ont en outre une susceptibilité accrue à l’obésité, au diabète et à certains cancers. Qu’est-ce qui les différencie ?
Il ne s’agit pas d’une mutation affectant la séquence de leur ADN, mais bien d’une marque épigénétique portée par les souris brunes, qui éteint le gène agouti.
Or on observe que la proportion de souriceaux bruns est plus importante dans la descendance des mères brunes que dans celle des mères au pelage jaune : ceci suggère que les mères brunes peuvent transmettre à leur descendance la marque épigénétique qui éteint le gène agouti.» (INSERM)
L’épigénétique et les maladies.
L’épigénétique intervenant entre autre lors de la division cellulaire contribue à la progression de certaines maladies humaines. La surexpression ou l’inhibition de certains gènes peuvent favoriser le développement de pathologies, tels les cancers.
Aujourd’hui de nombreuses recherches tendent à montrer l’implication de l’épigénétique dans le développement et la progression constante de certaines maladies métaboliques, l’obésité, le diabète de type 2… ou de pathologies neuro-dégénératives, Alzheimer, Parkinson…
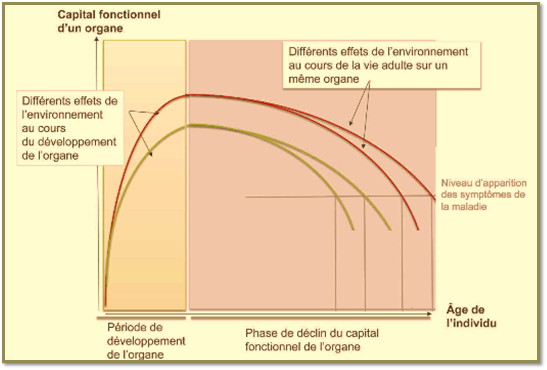
On sait que l’exposition in utéro du fœtus, à des facteurs de risques, toxiques environnementaux, stress, mauvais mode de vie…, le prédispose à développer à l’âge adulte des maladies chroniques.
Institut de Recherche en Santé Publique (IRSP)
Question de santé publique N° 18 Septembre 2012
Actuellement, on sait décrire l’épigénome (ensemble des modifications épigénétiques) d’un individu, cela devrait permettre de mieux appréhender l’implication de l’épigénétique dans les maladies humaines.
Le décryptage de ces mécanismes par lesquels les modifications épigénétiques fixent la mémoire des expositions environnementales subies précocement et l’intégration des résultats de ces recherches entraînera des changements majeurs en santé publique dans la prévention et la prise en charge des maladies chroniques de l’adulte les plus fréquentes (obésité, diabète, maladies cardiovasculaires, cancer).
La “DOHaD” est une approche transversale de la santé et donc de la médecine et de la recherche. La science avance, et tous les jours de plus en plus de liens entre des événements précoces et la santé à l’âge adulte apparaissent.
Cette nouvelle vision propose de nouvelles approches, un regard nouveau pour la santé globale, la prévention des maladies chroniques et l’optimisation du capital-santé des enfants et des générations à venir.
Institut de Recherche en Santé Publique (IRSP)
Question de santé publique N° 18 Septembre 2012

